
HÓA HỌC TÌM HIỂU VỀ LƯU HUỲNH
LƯU HUỲNH
I. Mục tiêu:
-Sự biến đổi cấu tạo phân tử và tính chất vật lí của lưu huỳnh theo nhiệt độ.
-Vì sao lưu huỳnh vừa có tính oxi hóa, vừa có tính khử.
-So sánh được những điểm giống nhau và khác nhau về tính chất hóa học
giữa oxi và lưu huỳnh.
II. Trọng tâm: Tính chất hóa học của lưu huỳnh.
III. Chuẩn bị:
-GV: Tranh mô tả cấu tạo tinh thể và tính chất vật lí của lưu huỳnh, bảng
tuần hoàn các nguyên tố hóa học
-HS: Tìm hiểu bài trước ở nhà
IV. Hoạt động dạy học:
Hoạt động của giáo viên và học sinh Nội dung
Hoạt động 1:
-Em hãy trình bày tính chất hoá học
của oxi
-Nêu những điểm khác nhau giữa
oxi và ozon.
Hoạt động 2:
GV: Treo bảng tuần hoàn lên bảng, yêu
cầu HS cho biết vị trí của lưu huỳnh,
viết cấu hình electron, nhận xét số
electron lớp ngoài cùng.
.
Hoạt động 3:
GV: Hướng dẫn HS quan sát tranh vẽ
tinh thể hai dạng thù hình của lưu
huỳnh, từ đó yêu cấu HS rút ra nhận
xét về tính bền, nhiệt độ sôi, nhiệt độ
nóng chảy.
GV: yêu cầu HS xem thêm SGK
Hoạt động 4:
GV: Mô tả thí nghiệm: đun ống nghiệm
đựng lưu huỳnh trên ngọn lửa đèn cồn,
yêu cầu học sinh nhận xét.
GV: Bổ xung để đơn giản trong các
phương trình phản ứng ta dùng ký hiệu
S mà không dùng S8.
Hoạt động 5:
GV: Yêu cầu HS xác định số oxi hoá
I. Vị trí, cấu hình electron của nguyên
tử
-Vị trí: + Z = 16
+ Chu kì 3
+ Nhóm VI
- Cấu hình electron:
1s22s22p63s23p4
=> Lớp ngoài cùng có 6 electron trong
đó có 2 electron độc thân.
II. Tính chất vật lý
1. Hai dạng thù hình của lưu huỳnh
-Lưu huỳnh có hai dạng thù hình: lưu
huỳnh tà phương (S), lưu huỳnh đơn tà
(S).
Kết luận: Hai dạng thù hình khác nhau
về tính chất vật lý, có thể biến đổi qua
lại với nhau tuỳ theo nhiệt độ.
2. Ảnh hưởng của nhiệt độ đến tính
chất vật lý
Rắn Lỏng Quánh Hơi
Vàng Vàng Nâu đỏ Nâu đỏ
III. Tính chất hoá học của lưu huỳnh
S có các số oxi hóa sau: -2, 0, +4, +6 =>
Đơn chất lưu huỳnh vừa có tính oxi hóa,
1190
của lưu huỳnh trong các chất: H2S, S,
SO2, H2SO4
GV: gợi ý HS dự đoán tính chất của
lưu huỳnh.
Hoạt động 6:
GV: Mô ta thí nghiệm: Cu + S ,yêu cấu
HS viết phương trình phản ứng.
GV: Yêu cầu học sinh viết phương
trình phản ứng Fe tác dụng với S, H2
tác dụng với S. Xác định sự thay đổi số
oxi hoá của lưu huỳnh từ đó rút ra nhận
xét?
GV: Bổ xung Hg tác dụng với S ngay ở
nhiệt độ thường.
Hoạt động 7:
GV: Hướng dẫn HS viết phương trình
hoá học của phản ứng S tác dụng với
O2, F2. Yêu cầu HS xác định sự thay
đổi về số oxi hoá của lưu huỳnh, từ đó
cho nhận xét?
Hoạt động 8:
GV: Hướng dẫn HS đọc SGK và liên
hệ thực tiễn rút ra những ứng dụng của
lưu huỳnh.
GV: yêu cầu HS nghiên cứu thêm
SGK.
Hoạt động 9:
GV: Yêu cầu các em nghiên cứu SGK
và tóm tắt trạng thái tự nhiên và sản
xuất lưu huỳnh?
vừa có tính khử.
1. Lưu huỳnh tác dụng với kim lọai
và hiđro
+ Tác dụng với kim loại:
0 0 -2
S + Cu
o
t
CuS
0 0 -2
S + Fe
o
t
FeS
+ Tác dụng với H2:
0 0 -2
S + H2
H2S
=> Trong các phản ứng này S thể hiện
tính oxi hóa:
0 -2
S+ 2e
S.
S tác dụng với Hg ngay ở nhiệt độ
thường:
0 0 -2
S + Hg
HgS
2. Tác dụng với phi kim
- ở nhiệt độ thích hợp, S tác dụng được
với nhiều phi kim mạnh hơn:
0 0 +4 -2
S + O2
o
t
SO2.
0 0 +6-1
S + F2
o
t
SF6.
=> Trong các phản ứng này, S thể hiện
tính khử:
0 +4
S
S + 4e
0 +6
S
S + 6e.
IV. ứng dụng của lưu huỳnh
- Dùng để sản xuất axit H2SO4 :
S
SO2
SO3
H2SO4
- Lưu hóa cao su, sản xuất diêm, dược
phẩm, chất trừ sâu, phẩm nhuộm,…
(SGK).
V. Trạng thái tự nhiên và sản xuất
lưu huỳnh
+ Trạng thái tự nhiên:
-Có nhiều ở dạng đơn chất tạo thành
các mỏ lớn trong lòng đất.
-ở dạng hợp chất như muối sunfat,
muối sunfua,…
+ Khai thác lưu huỳnh trong tự nhiên:
dùng thiết bị đặc biệt.
IV. cũng cố
-GV: nhắc lại các kiến thức trong bài, yêu cầu HS nắm vững tính chất hóa
học của lưu huỳnh và làm bài tập ở nhà
có thể bạn quan tâm

HÓA HỌC TÌM HIỂU VỀ HIĐROSUNFUA, LƯU HUỲNH ĐIOXIT, LƯU HUỲNH TRIOXIT(...
2
1.029
375
Giáo án, bài giảng lớp 10
2
(New)

HÓA HỌC TÌM HIỂU VỀ HIĐROSUNFUA, LƯU HUỲNH ĐIOXIT, LƯU HUỲNH TRIOXIT(T...
2
947
388
Giáo án, bài giảng lớp 10
2
(New)

HÓA HỌC TÌM HIỂU VỀ OXI - LƯU HUỲNH ( LUYỆN TẬP)
3
1.128
378
Giáo án, bài giảng lớp 10
3
(New)

HÓA HỌC TÌM HIỂU VỀ TÍNH CHẤT CỦA OXI, LƯU HUỲNH
2
922
405
Giáo án, bài giảng lớp 10
2
(New)

HÓA HỌC TÌM HIỂU VỀ NHÓM OXI – LƯU HUỲNH- T1 ( LUYỆN TẬP)
2
1.005
417
Giáo án, bài giảng lớp 10
2
(New)

HÓA HỌC TÌM HIỂU VỀ NHÓM OXI – LƯU HUỲNH - T2 ( LUYỆN TẬP)
2
952
372
Giáo án, bài giảng lớp 10
2
(New)

HÓA HỌC TÌM HIỂU VỀ TÍNH CHẤT CỦA LƯU HUỲNH ( THỰC HÀNH)
2
1.107
400
Giáo án, bài giảng lớp 10
2
(New)
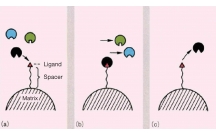
Xác định các điều kiện tối ưu trong việc dùng cột sắc ký ái lực miễn d...
50
963
424
Kỹ thuật
50
(New)
thông tin tài liệu
HÓA HỌC TÌM HIỂU VỀ LƯU HUỲNH
trí, cấu hình electron của nguyên tử
-Vị trí: + Z = 16
+ Chu kì 3
+ Nhóm VI
- Cấu hình electron:
1s22s22p63s23p4
=> Lớp ngoài cùng có 6 electron trong đó có 2 electron độc thân.
II. Tính chất vật lý
1. Hai dạng thù hình của lưu huỳnh
-Lưu huỳnh có hai dạng thù hình: lưu huỳnh tà phương (S), lưu huỳnh đơn tà (S).
Kết luận: Hai dạng thù hình khác nhau về tính chất vật lý, có thể biến đổi qua lại với nhau tuỳ theo nhiệt độ.
2. Ảnh hưởng của nhiệt độ đến tính chất vật lý
Rắn Lỏng Quánh Hơi
Vàng Vàng Nâu đỏ Nâu đỏ
III. Tính chất hoá học của lưu huỳnh
S có các số oxi hóa sau: -2, 0, +4, +6 => Đơn chất lưu huỳnh vừa có tính oxi hóa, vừa có
Mở rộng để xem thêm
từ khóa liên quan
tài liệu mới trong mục này
tài liệu hot trong mục này
tài liệu giúp tôi
Nếu bạn không tìm thấy tài liệu mình cần có thể gửi yêu cầu ở đây để chúng tôi tìm giúp bạn!
xem nhiều trong tuần
70 câu hỏi trắc nghiệm luyện thi chứng chỉ tin A
Đề thi và lời giải môn xác suất thống kê của trường Học viện ngân hàng
Địa lý 12 Phát triển cây công nghiệp lâu năm Tây Nguyên
Bài tập nâng cao Tiếng Việt lớp 2: Chính tả
Tiểu luận: Vị trí, vai trò, nhiệm vụ của người Đảng viên với ĐCSVN- Phấn đấu, rèn luyện và tuyên truyền nhân dân của người Đảng viên
Giáo trình Quản trị học của Đại học kinh tế quốc dân
yêu cầu tài liệu
Giúp bạn tìm tài liệu chưa có
×



