
Hướng dẫn Giải bài tập Hóa lớp 9: Một số Bazơ quan trọng
H ng d n Gi i bài t p Hóa l p 9: M t s Baz quan tr ngướ ẫ ả ậ ớ ộ ố ơ ọ
Bài 1. (Trang 27 SGK Hóa 9 ch ng 1)ươ
Có 3 l không nhãn, m i l đ ng ch t r n sau: NaOH, Ba(OH)2, NaCl. Hãy trình bàyọ ỗ ọ ự ấ ắ
cách nh n bi t ch t đ ng trong m i l b ng ph ng pháp hóa h c. Vi t các ph ngậ ế ấ ự ỗ ọ ằ ươ ọ ế ươ
trình hóa h c (n u có).ọ ế
H ng d n gi i bài 1:ướ ẫ ả
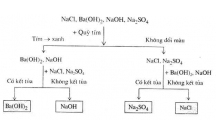
Hòa tan m u th t ng ch t vào n c đ t o thành các dung d ch t ng ng. Cho quỳẫ ử ừ ấ ướ ể ạ ị ươ ứ
tím vào m i dung d ch: N u quỳ tím chuy n sang màu xanh là NaOH và Ba(OH)ỗ ị ế ể 2, n uế
quỳ tím không đ i màu là NaCl.ổ
Nh v y đã tìm đ c Nacl, ti p t c tìm cách nh n bi t: NaOH và Ba(OH)ư ậ ượ ế ụ ậ ế 2
D n khí COẫ2 vào hai dung d ch baz còn l i: N u có k t t a xu t hi n là Ba(OH)2 n uị ơ ạ ế ế ủ ấ ệ ế
không k t t a là NaOH.ế ủ
Ba(OH)2 + CO2 → BaCO3↓ + H2O
2NaOH + CO2 → Na2CO3 + H2O
Bài 2. (Trang 27 SGK Hóa 9 ch ng 1)ươ
Có nh ng ch t sau: Zn, Zn(OH)2, NaOH, Fe(OH)ữ ấ 3, CuSO4, NaCl, HCl.
Hãy ch n ch t thích h p đi n vào m i s đ ph n ng sau và l p ph ng trình h c:ọ ấ ợ ề ỗ ơ ồ ả ứ ậ ươ ọ
a) ….. → Fe2O3 + H2O;
b) H2SO4 + … → Na2SO4 + H2O;
c) H2SO4 + … → ZnSO4 + H2O;
d) NaOH + …. → NaCl + H2O;
e) ….. + CO2 → Na2CO3 + H2O.
H ng d n gi i bài 2:ướ ẫ ả
a) 2Fe(OH)3 → Fe2O3 + 3H2O;
b) H2SO4 + 2NaOH → Na2SO4 + 2H2O;
c) H2SO4 + Zn(OH)2 → ZnSO4 + 2H2O;
d) NaOH + HCl → NaCl + H2O;
e) 2NaOH + CO2 → Na2CO3 + H2O
Bài 3. (Trang 27 SGK Hóa 9 ch ng 1)ươ
D n t t 1,568 lít khí COẫ ừ ừ 2 (đktc) vào m t dung d ch có hòa tan 6,4 gam NaOH, s nộ ị ả
ph m là mu i Naẩ ố 2CO3.
a) Ch t nào đã l y d và d là bao nhiêu (lít ho c gam)?ấ ấ ư ư ặ
b) Hãy xác đ nh kh i l ng mu i thu đ c sau ph n ng.ị ố ượ ố ượ ả ứ
L i g i.ờ ả
S mol: nốCO2 =1,568/22,4 = 0,07 mol; nNaOH =6,4/40 = 0,16 mol
Ph ng trình hóa h c:ươ ọ
2NaOH + CO2 → Na2CO3 + H2O
Bđ: 0,07 0,16 0 (mol)
P : 0,07 → 0,14 0,07ứ
Sp : 0 0,02 0,07ứ
a) Ch t còn d là NaOH và d : 0,02×40 = 0,8 gấ ư ư
b) Kh i l ng mu i Naố ượ ố 2CO3 t o thành là: 0,07×106 = 7,42 g.ạ
có thể bạn quan tâm
Hướng dẫn Giải bài tập Hóa lớp 9: Tính chất hóa học của Bazơ
3
892
329
Giải bài tập các môn
3
(New)

Hướng dẫn giải bài tập Hóa học 9 - Thực hành: Tính chất hóa học của ba...
2
867
345
Giải bài tập các môn
2
(New)

Hướng dẫn Giải bài tập SGK Hóa lớp 9: Một số oxit quan trọng
4
773
368
Giải bài tập các môn
4
(New)

Hướng dẫn Giải bài tập SGK Hóa lớp 9: Một số axit quan trọng
6
758
347
Giải bài tập các môn
6
(New)
HƯỚNG DẪN GIẢI BÀI TẬP HÓA LỚP 9: MỘT SỐ MUỐI QUAN TRỌNG
3
1.102
407
Giáo án, bài giảng khác
3
(New)

Tóm tắt kiến thức cơ bản và giải bài tập Hóa học lớp 11: Axit, bazơ và...
3
1.088
344
Giải bài tập các môn
3
(New)

Nghiên cứu là đề xuất định hướng, giải pháp có cơ sở khoa học, thực ti...
143
1.048
341
Kinh tế quản lý
143
(New)

Tóm tắt kiến thức cơ bản và giải bài tập Hóa học lớp 11: Sự điện li củ...
3
817
335
Giải bài tập các môn
3
(New)
thông tin tài liệu
Bài 1. (Trang 27 SGK Hóa 9 chương 1)
Có 3 lọ không nhãn, mỗi lọ đựng chất rắn sau: NaOH, Ba(OH)2, NaCl. Hãy trình bày cách nhận biết chất đựng trong mỗi lọ bằng phương pháp hóa học. Viết các phương trình hóa học (nếu có).
Hướng dẫn giải bài 1:
Hòa tan mẫu thử từng chất vào nước để tạo thành các dung dịch tương ứng. Cho quỳ tím vào mỗi dung dịch: Nếu quỳ tím chuyển sang màu xanh là NaOH và Ba(OH)2, nếu quỳ tím không đổi màu là NaCl.
Như vậy đã tìm được Nacl, tiếp tục tìm cách nhận biết: NaOH và Ba(OH)2
Dẫn khí CO2 vào hai dung dịch bazơ còn lại: Nếu có kết tủa xuất hiện là Ba(OH)2 nếu không kết tủa là NaOH.
Ba(OH)2 + CO2 → BaCO3↓ + H2O
2NaOH + CO2 → Na2CO3 + H2O
Mở rộng để xem thêm
tài liệu mới trong mục này
tài liệu hot trong mục này
tài liệu giúp tôi
Nếu bạn không tìm thấy tài liệu mình cần có thể gửi yêu cầu ở đây để chúng tôi tìm giúp bạn!
xem nhiều trong tuần
Địa lý 12 Phát triển cây công nghiệp lâu năm Tây Nguyên
Đề thi và lời giải môn xác suất thống kê của trường Học viện ngân hàng
Giáo trình Quản trị học của Đại học kinh tế quốc dân
MẪU GIẤY THI A4
Bài tập ôn tập cuối tuần lớp 2: Tuần 31
MẪU GIỚI THIỆU CHUYỂN SINH HOẠT HỘI
yêu cầu tài liệu
Giúp bạn tìm tài liệu chưa có
×



