
Home
Giáo dục đào tạo
Giải bài tập các môn
Tóm tắt kiến thức cơ bản và Giải bài tập Hóa học lớp 11: Axit photphoric và muối photphat
Tóm tắt kiến thức cơ bản và Giải bài tập Hóa học lớp 11: Axit photphoric và muối photphat
Tóm t t ki n th c c b nắ ế ứ ơ ả và Gi i bài t p Hóa h c l p 11: ả ậ ọ ớ Axit photphoric và
mu i photphatố
I. Tóm t t ki n th c c b n: Axit photphoric và mu i photphatắ ế ứ ơ ả ố
1. Photpho có đ âm đi n nh nên m c oxi hóa +5 nên Hộ ệ ỏ ở ứ 3PO4 khó b kh , không cóị ử
tính oxi hóa nh axit HNOư3.
2. Axit photphoric là ch t tinh th , trong su t, không màu, r t háo n c, tan t t trongấ ể ố ấ ướ ố
n c.ướ
3. Axit H3PO4 là axit ba n c, có đ m nh trung bình. Trong dung d ch đi n li y u theoấ ộ ạ ị ệ ế
ba n c (ch y u phân li theo n c 1, n c 2 kém h n và n c 3 r t y u).ấ ủ ế ấ ấ ơ ấ ấ ế
Dung d ch Hị3PO4 có nh ng tính ch t chung c a axit, nh làm đ i màu quỳ tím thành đ ,ữ ấ ủ ư ổ ỏ
tác d ng v i oxit baz , baz , mu i, kim lo i có tính kh m nh h n H,… Khi tác d ngụ ớ ơ ơ ố ạ ử ạ ơ ụ
v i oxit baz ho c baz , tùy theo l ng ch t tác d ng mà axit photphoric t o ra mu iớ ơ ặ ơ ượ ấ ụ ạ ố
trung hòa, mu i axit ho c h n h p mu i.ố ặ ỗ ợ ố
4. - Trong phòng thí nghi m, axit photphoric đ c đi u ch b ng cách dùng HNOệ ượ ề ế ằ 3 đ cặ
oxi hóa photpho:
P + 5HNO3 → H3PO4 + 5NO2 + H2O
- Trong công nghi p: ệĐi u ch t qu ng photphorit ho c qu ng apatit và axit Hề ế ừ ặ ặ ạ 2SO4:
Ca3(PO4)2 + 3H2SO4 (đ c)ặ → 3CaSO4 + 2H3SO4
- Đ đi u ch Hể ề ế 3PO4 có đ tinh khi t và n ng đ cao h n, ng i ta đ t cháy photphoộ ế ồ ộ ơ ườ ố
đ đ c Pể ượ 2O5, r i cho Pồ2O5 tác dunngj v i n c.ớ ướ
4P + 5O2 → t0 2P2O5
P2O5 + 3H2O → 2H3PO4.
5. M t l ng l n axit photphoric s n xu t ra đ c dùng đ đi u ch các mu i photphatộ ượ ớ ả ấ ượ ể ề ế ố
và đ s n xu phân lân.ể ả ẩ
6. Mu i photphat là mu i c a axit photphoric. Axit photphoric t o ra ba lo i mu i:ố ố ủ ạ ạ ố
mu i photphat trung hòa và hai mu i photphat axit. T t c các mu i đihiđrophotphatố ố ấ ả ố
đ u tan trong n c. Các mu i hiđrophotphat và photphat trung hòa ch có mu i natri,ề ướ ố ỉ ố
kali, amoni là d tan, còn mu i c a các kim lo i khác đ u không tan ho c ít tan trongễ ố ủ ạ ề ặ
n c. Các mu i photphat tan b th y phân cho môi tr ng ki m: POướ ố ị ủ ườ ề 43- + H2O ⇔
HPO42- + OH-
7. Thu c th đ nh n bi t ion POố ử ể ậ ế 43- trong dung d ch mu i photphat và b c nitrat.ị ố ạ
II. Gi i bài t p trang 53, 54 SGK Hóa h c l p 11ả ậ ọ ớ
Bài 1. Vi t ph ng trình hóa h c d ng phân t và d ng ion rút g n c a ph n ng gi aế ươ ọ ạ ử ạ ọ ủ ả ứ ữ
H3PO4 v i l ng d c a:ớ ượ ư ủ
a) BaO b) Ca(OH)2 c) K2CO3
Tr l i:ả ờ Do các ch t a) BaO, b) Ca(OH)ấ2, c) K2CO3 l y d nên khi tác d ng v iấ ư ụ ớ
H3PO4 mu i t o thành là mu i photphat trung hòa:ố ạ ố
a) 3BaO + 2H3PO4 → Ba3(PO4)2 + 3H2O
b) 3Ca(OH)2 + 2H3PO4 → Ca3(PO4)2 + 6H2O
c) 3K2CO3 + 2H3PO4 → 2K3PO4 + 3CO2 + 3H2O
Bài 2. Nêu nh ng đi m gi ng nhau và khác nhau v tính ch t hóa h c gi a axit nitricữ ể ố ề ấ ọ ữ
và axit photphoric. D n ra nh ng ph n ng hóa h c đ minh h aẫ ữ ả ứ ọ ể ọ .
Tr l i:ả ờ
- Gi ng:ố
+ Trong dung d ch n c đ u đi n li ra ion Hị ướ ề ệ +
+ Đ u có th tác d ng v i kim lo i, oxit baz , baz , mu iề ể ụ ớ ạ ơ ơ ố
Ví d : Naụ2O + 2HNO3 → 2NaNO3 + H2O
3Na2O + 2H3PO4 → 2Na3PO4 + 3H2O
- Khác:
HNO3 có tính oxi hóa; H3PO4 không có tính oxi hóa
Ví d :ụ
C + 4HNO3 → CO2 + 4NO2 + 2H2O
Bài 3. Ph ng trình đi n li t ng c ng c a Hươ ệ ổ ộ ủ 3PO4 trong dung d ch là:ị H3PO4 3H⇔+ +
PO43-
Khi thêm HCl vào dung d ch,ị
A. Cân b ng trên chuy n d ch theo chi u thu n.ằ ể ị ề ậ
B. Cân b ng trên chuy n d ch theo chi u ngh ch.ằ ể ị ề ị
C. Cân b ng trên không b chuy n d ch.ằ ị ể ị
D. N ng đ POồ ộ 43- tăng lên.
Tr l i:ả ờ Theo nguyên lí chuy n dich cân b ng: ể ằ Cân b ng chuy n d ch theo h ng làmằ ể ị ướ
gi m tác đ ng vào h . Do đó khi thêm Hả ộ ệ + vào dung d ch, cân b ng trên chuy n d chị ằ ể ị
theo chi u ngh ch t o thành Hề ị ạ 3PO4.
=> Đáp án đúng là B
Bài 4. L p ph ng trình hóa h c sau đây:ậ ươ ọ
a) H3PO4 + K2HPO4 →
1 mol 1 mol
b) H3PO4 + Ca(OH)2 →
1 mol 1 mol
c) H3PO4 + Ca(OH)2 →
2 mol 1 mol
d) H3PO4 + Ca(OH)2 →
2 mol 3 mol
Tr l i: ả ờ Căn c vào t l mol đ vi t s n ph m t o thành r i cân b ng pthh:ứ ỉ ệ ể ế ả ẩ ạ ồ ằ
a) H3PO4 + K2HPO4 → 2KH2PO4
1 mol 1 mol
b) H3PO4 + Ca(OH)2 → CaHPO4 + 2H2O
1 mol 1 mol
c) H3PO4 + Ca(OH)2 → Ca(H2PO4)2 + 2H2O
2 mol 1 mol
d) H3PO4 + Ca(OH)2 → Ca3(PO4)2 + 6H2O
2 mol 3 mol
Bài 5. Đ thu đ c mu i photphat trung hòa, c n l y bao nhiêu ml dung dich NaOHể ượ ố ầ ấ
1,00 M cho tác d ng v i 50,0 ml dung d ch Hụ ớ ị 3PO4 0,50 M?
Tr l i: ả ờ S mol Hố3PO4: 0,050 x 0,50 = 0,025 (mol).
H3PO4 + 3NaOH → Na3PO4 + 3H2O
1 mol 3 mol
0,025 mol 3 x 0,025 mol
Th tích dung d ch NaOH: 0,075 lít hay 75 mlể ị
có thể bạn quan tâm

Tóm tắt kiến thức cơ bản và giải bài tập Hóa học lớp 11: Axit, bazơ và...
3
1.083
341
Giải bài tập các môn
3
(New)

Tóm tắt kiến thức cơ bản và Giải bài tập Hóa học lớp 11: Axit nitric v...
4
767
319
Giải bài tập các môn
4
(New)

Tóm tắt kiến thức cơ bản và giải bài tập Hóa học lớp 11: Amoniac và mu...
4
775
333
Giải bài tập các môn
4
(New)
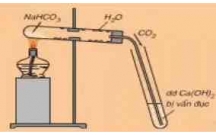
Giải bài tập Hóa Học 9: Axit cacbonic và muối cacbonat
2
931
445
Giải bài tập các môn
2
(New)
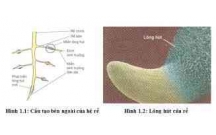
Tóm tắt kiến thức và Giải bài tập Sinh học lớp 11: Sự hấp thụ nước và...
3
584
287
Giải bài tập các môn
3
(New)

Tóm tắt kiến thức cơ bản và giải bài tập Hóa học lớp 11: Sự điện li củ...
3
812
334
Giải bài tập các môn
3
(New)

HÓA HỌC 8 LÝ THUYẾT VÀ BÀI TẬP AXIT – BAZƠ - MUỐI
11
1.342
355
Giáo án, bài giảng lớp 8
11
(New)

HÓA HỌC TÌM HIỂU VỀ AXIT SUNFURIC, MUỐI SUNFAT (T2)
2
1.209
384
Giáo án, bài giảng lớp 10
2
(New)
thông tin tài liệu
I. Tóm tắt kiến thức cơ bản: Axit photphoric và muối photphat
1. Photpho có độ âm điện nhỏ nên ở mức oxi hóa +5 nên H3PO4 khó bị khử, không có tính oxi hóa như axit HNO3.
2. Axit photphoric là chất tinh thể, trong suốt, không màu, rất háo nước, tan tốt trong nước.
3. Axit H3PO4 là axit ba nấc, có độ mạnh trung bình. Trong dung dịch điện li yếu theo ba nấc (chủ yếu phân li theo nấc 1, nấc 2 kém hơn và nấc 3 rất yếu).
Dung dịch H3PO4 có những tính chất chung của axit, như làm đổi màu quỳ tím thành đỏ, tác dụng với oxit bazơ, bazơ, muối, kim loại có tính khử mạnh hơn H,… Khi tác dụng với oxit bazơ hoặc bazơ, tùy theo lượng chất tác dụng mà axit photphoric tạo ra muối trung hòa, muối axit hoặc hỗn hợp muối.
4. - Trong phòng thí nghiệm, axit photphoric được điều chế bằng cách dùng HNO3 đặc oxi hóa photpho:
P + 5HNO3 → H3PO4 + 5NO2 + H2O
- Trong công nghiệp: Điều chế từ quặng photphorit hoặc quạng apatit và axit H2SO4:
Ca3(PO4)2 + 3H2SO4 (đặc) → 3CaSO4 + 2H3SO4
- Để điều chế H3PO4 có độ tinh khiết và nồng độ cao hơn, người ta đốt cháy photpho để được P2O5, rồi cho P2O5 tác dunngj với nước.
4P + 5O2 → t0 2P2O5
P2O5 + 3H2O → 2H3PO4.
5. Một lượng lớn axit photphoric sản xuất ra được dùng để điều chế các muối photphat và để sản xuẩ phân lân.
6. Muối photphat là muối của axit photphoric. Axit photphoric tạo ra ba loại muối: muối photphat trung hòa và hai muối photphat axit. Tất cả các muối đihiđrophotphat đều tan trong nước. Các muối hiđrophotphat và photphat trung hòa chỉ có muối natri, kali, amoni là dễ tan, còn muối của các kim loại khác đều không tan hoặc ít tan trong nước. Các muối photphat tan bị thủy phân cho môi trường kiềm: PO43- + H2O ⇔ HPO42- + OH-
.....
Mở rộng để xem thêm
tài liệu mới trong mục này
tài liệu hot trong mục này
tài liệu giúp tôi
Nếu bạn không tìm thấy tài liệu mình cần có thể gửi yêu cầu ở đây để chúng tôi tìm giúp bạn!
xem nhiều trong tuần
CHÍNH SÁCH PHÁT TRIỂN: Bài 3 - Lý thuyết phát triển
Tiếng Anh lớp 3 - Đề thi học kỳ 2 trường Tiểu Học Nguyễn Khuyến, Đắk Lắk
Hướng dẫn chuyển Bookmarks từ Firefox sang Chrome
Giải bài tập SBT Tiếng Anh lớp 9 mới Unit 7
Làm gì để tránh biến chứng bệnh tiểu đường
CHÍNH SÁCH PHÁT TRIỂN: Bài 1 - Mô thức phát triển và các vấn đề của CSPT
yêu cầu tài liệu
Giúp bạn tìm tài liệu chưa có
×



