
Home
Giáo dục đào tạo
Giải bài tập các môn
Tóm tắt lý thuyết và hướng dẫn giải bài tập hóa học 10: Sự biến đổi tuần hoàn cấu hình electron nguyên tử của các nguyên tố hóa học
Tóm tắt lý thuyết và hướng dẫn giải bài tập hóa học 10: Sự biến đổi tuần hoàn cấu hình electron nguyên tử của các nguyên tố hóa học
Tóm t t lý thuy t và h ng d n gi i bài t p hóa h c 10: S bi n đ i tu n hoàn cắ ế ướ ẫ ả ậ ọ ự ế ổ ầ ấu
hình electron nguyên t c a các nguyên t hóa h cử ủ ố ọ
A. Lý thuy t c n nh vế ầ ớ ề s bi n đ i tu n hoàn cự ế ổ ầ ấu hình electron nguyên t c aử ủ
các nguyên t hóa h c.ố ọ
– Sau m i chu kì, c u hình electron nguyên t các nguyên t nhóm A l p ngoài cùngỗ ấ ử ố ở ớ
đ c l p l i nh chu kì tr c. Ta g i đó là s bi n đ i tu n hoàn.ượ ặ ạ ư ở ướ ọ ự ế ổ ầ
– S bi n đ i tu n hoàn v c u hình electron l p ngoài cùng c a nguyên t các nguyênự ế ổ ầ ề ấ ớ ủ ử
t chính là nguyên nhân c a s bi n đ i tu n hoàn v tính ch t các nguyên t .ố ủ ự ế ổ ầ ề ấ ố
– S gi ng nhau v c u hình electron l p ngoài cùng c a nguyên t là nguyên nhân c aự ố ề ấ ớ ủ ử ủ
s gi ng nhau v tính ch t hóa h c c a các nguyên t trong cùng m t nhóm A.ự ố ề ấ ọ ủ ố ộ
B. Gi i bài t p SGK Hóa l p 10 ch ng 2 trang 41.ả ậ ớ ươ
Bài 1. (SGK trang 41 Hóa l p 10)ớ
Các nguyên t thu c cùng m t nhóm A có tính ch t hóa h c t ng t nhau, vì vố ộ ộ ấ ọ ươ ự ỏ
nguyên t c a các nguyên t nhóm A cóử ủ ố
A. s electron nh nhauố ư
B. s l p electron nh nhauố ớ ư
C. s electron thu c l p ngoài cùng nh nhau.ố ộ ớ ư
D. cùng s electron s hay p.ố
Ch n đáp án đúng.ọ
Đáp án bài 1:
Ch n câu C:ọ s electron thu c l p ngoài cùng nh nhau.ố ộ ớ ư
Bài 2. (SGK trang 41 Hóa l p 10)ớ
S bi n thiên tính ch t c a các nguyên t thu c chu kì sau đ c l p l i t ng t nhự ế ấ ủ ố ộ ượ ặ ạ ươ ự ư
chu kì tr c là do:ướ
A. S l p l i tính ch t kim lo i c a các nguyên t chu kì sau so v i chu kì tr c.ự ặ ạ ấ ạ ủ ố ở ớ ướ
B. S l p l i tính ch t phi kim c a các nguyên t chu kì sau so v i chu kì tr c.ự ặ ạ ấ ủ ố ở ớ ướ
C. S l p l i c u hình electron l p ngoài cùng c a nguyên t các nguyên t chu kìự ặ ạ ấ ớ ủ ử ố ở
sau so v i chu kì tr c ( ba chu kì đ u).ớ ướ ở ầ
D. S l p l i tính ch t hóa h c c a các nguyên t chu kì sau so v i chu kì tr c.ự ặ ạ ấ ọ ủ ố ở ớ ướ
Ch n đáp án đúng.ọ
Đáp án bài 2:
C đúng
S l p l i c u hình electron l p ngoài cùng c a nguyên t các nguyên t chu kì sauự ặ ạ ấ ớ ủ ử ố ở
so v i chu kì tr c vì có s bi n đ i electron l p ngoài cùng c a nguyên t các nguyênớ ướ ự ế ổ ớ ủ ử
t chu kì sau gi ng nh chu kì tr c khi đi n tích h t nhân tăng d n.ố ố ư ướ ệ ạ ầ
Bài 3. (SGK trang 41 Hóa l p 10)ớ
Nh ng nguyên t thu c nhóm A nào là các nguyên t s, nguyên t p? S electron thu cữ ố ộ ố ố ố ộ
l p ngoài cùng trong nguyên t c a các nguyên t s và p khác nhau th nào?ớ ử ủ ố ế
Đáp án và h ng d n ướ ẫ gi iả bài 3:
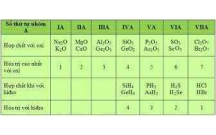
– Các electron hóa tr c a các nguyên t thu c nhóm IA, IIA là electron s. Các nguyên tị ủ ố ộ ố
đó đ c g i là nguyên t s.ượ ọ ố
– Các electron hóa tr c a các nguyên t thu c nhóm IIIA, IVA, VA, VIA, VIIA, VIIIA làị ủ ố ộ
các electron s và p. Các nguyên t đó đ c g i là nguyên t p.ố ượ ọ ố
– S electron thu c l p ngoài cùng trong nguyên t c a các nguyên t s là 1 và 2. Số ộ ớ ử ủ ố ố
electron thu c l p ngoài cùng trong nguyên t c a các nguyên t p là 3, 4, 5, 6, 7, 8.ộ ớ ử ủ ố
Bài 4. (SGK trang 41 Hóa l p 10)ớ
Nh ng nguyên t nào đ ng đ u các chu kìữ ố ứ ầ ? C u hình electron nguyên t c a cácấ ử ủ
nguyên t đó có đ c đi m chung gìố ặ ể ?
Đáp án và h ng d n ướ ẫ gi i bài 4:ả
Nh ng nguyên t kim lo i ki m đ ng đ u chu kì. Tr chu kì 1, hiđro không ph i là kimữ ố ạ ề ứ ầ ừ ả
lo i ki m. C u hình electron c a nguyên t các nguyên t kim lo i ki m có 1 electronạ ề ấ ủ ử ố ạ ề
l p ngoài cùng.ớ
Bài 5. (SGK trang 41 Hóa l p 10)ớ
Nh ng nguyên t nào đ ng cu i các chu kìữ ố ứ ố ? C u hình electron c a nguyên t c a cácấ ủ ử ủ
nguyên t đó có đ c đi m chung gìố ặ ể ?
Đáp án và h ng d n ướ ẫ gi i bài 5:ả
Nh ng nguyên t khí hi m đ ng cu i chu kì. C u hình electron c a nguyên t cácữ ố ế ứ ố ấ ủ ử
nguyên t khí hi m có 8 electron l p ngoài cùng (riêng He có 2e).ố ế ở ớ
Bài 6. (SGK trang 41 Hóa l p 10)ớ
M t nguyên t chu kì 3, nhóm VIA trong b ng tu n hoàn các nguyên t hóa h c. H i:ộ ố ở ả ầ ố ọ ỏ
a) Nguyên t c a nguyên t đó có bao nhiêu electron l p electron ngoài cùngử ủ ố ở ớ ?
b) Các electron ngoài cùng n m l p electron th m yằ ở ớ ứ ầ ?
c) Vi t c u hình electron nguyên t c a nguyên t trên.ế ấ ử ủ ố
Đáp án và h ng d n ướ ẫ gi i bài 6:ả
a) Nguyên t c a nguyên t có 6 electron l p ngoài cùng.ử ủ ố ở ớ
b) C u hình electron l p ngoài cùng n m l p th ba.ấ ớ ằ ở ớ ứ
c) C u hình electron c a nguyên t : 1sấ ủ ố 22s22p63s23p4.
Bài 7. (SGK trang 41 Hóa l p 10)ớ
M t s nguyên t có c u hình electron c a nguyên t nh sau:ộ ố ố ấ ủ ử ư
1s22s22p41s22s22p3
1s22s22p63s23p11s22s22p63s23p5
a) Hãy xác đ nh s electron hóa tr c a t ng nguyên t .ị ố ị ủ ừ ử
b) Hãy xác đ nh v trí c a chúng (chu kì, nhóm) trong b ng tu n hoàn các nguyên t hóaị ị ủ ả ầ ố
h c.ọ
Đáp án và h ng d n ướ ẫ gi i bài 7:ả
a) 1s22s22p4: S electron hóa tr là 6.ố ị
1s22s22p3: S electron hòa tr là 5.ố ị
1s22s22p63s23p1: S electron hòa tr là 3.ố ị
1s22s22p63s23p5: S electron hòa tr là 7.ố ị
b) 1s22s22p4: Nguyên t thu c chu kì 2 nhóm VIA.ố ộ
1s22s22p3: Nguyên t thu c chu kì 2 nhóm VA.ố ộ
1s22s22p63s23p1: Nguyên t thu c chu kì 3 nhóm IIIA.ố ộ
1s22s22p63s23p5: Nguyên t thu c chu kì 3 nhóm VIIA.ố ộ
có thể bạn quan tâm

Hướng dẫn giải bài tập sách giáo khoa Hóa học lớp 10: Luyện tập bảng t...
5
867
359
Giải bài tập các môn
5
(New)
Tóm tắt lý thuyết và hướng dẫn giải bài tập SGk Hóa học 10: Sự biến đổ...
5
712
365
Giải bài tập các môn
5
(New)
Tóm tắt lý thuyết và hướng dẫn giải bài tập SGK Hóa học 10: Cấu hình e...
4
708
325
Giải bài tập các môn
4
(New)

Tóm tắt lý thuyết và hướng dẫn giải bài tập SGK Hóa học 10: Bảng tuần...
5
821
365
Giải bài tập các môn
5
(New)

Hướng dẫn giải bài tập sách giáo khoa Học học lớp 10: Ý nghĩa của bảng...
3
696
320
Giải bài tập các môn
3
(New)

Giải bài tập Hóa lớp 9: Sơ lược về bảng tuần hoàn các nguyên tố hoá họ...
5
1.066
413
Giải bài tập các môn
5
(New)
Tóm tắt lý thuyết và hướng dẫn giải bài tập SGK Hóa học 10: Hạt nhân n...
5
777
357
Giải bài tập các môn
5
(New)

HÓA HỌC TÌM HIỂU VỀ BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC (T1)
3
1.108
359
Giáo án, bài giảng lớp 10
3
(New)
thông tin tài liệu
A. Lý thuyết cần nhớ về sự biến đổi tuần hoàn cấu hình electron nguyên tử của các nguyên tố hóa học.
– Sau mỗi chu kì, cấu hình electron nguyên tử các nguyên tố nhóm A ở lớp ngoài cùng được lặp lại như ở chu kì trước. Ta gọi đó là sự biến đổi tuần hoàn.
– Sự biến đổi tuần hoàn về cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố chính là nguyên nhân của sự biến đổi tuần hoàn về tính chất các nguyên tố.
– Sự giống nhau về cấu hình electron lớp ngoài cùng của nguyên tử là nguyên nhân của sự giống nhau về tính chất hóa học của các nguyên tố trong cùng một nhóm A.
B. Giải bài tập SGK Hóa lớp 10 chương 2 trang 41.
Bài 1. (SGK trang 41 Hóa lớp 10)
Các nguyên tố thuộc cùng một nhóm A có tính chất hóa học tương tự nhau, vì vỏ nguyên tử của các nguyên tố nhóm A có
A. số electron như nhau
B. số lớp electron như nhau
C. số electron thuộc lớp ngoài cùng như nhau.
D. cùng số electron s hay p.
Chọn đáp án đúng.
Đáp án bài 1:
Chọn câu C: số electron thuộc lớp ngoài cùng như nhau.
.....
Mở rộng để xem thêm
tài liệu mới trong mục này
tài liệu hot trong mục này
tài liệu giúp tôi
Nếu bạn không tìm thấy tài liệu mình cần có thể gửi yêu cầu ở đây để chúng tôi tìm giúp bạn!
xem nhiều trong tuần
Địa lý 12 Phát triển cây công nghiệp lâu năm Tây Nguyên
Đề thi và lời giải môn xác suất thống kê của trường Học viện ngân hàng
Giáo trình Quản trị học của Đại học kinh tế quốc dân
MẪU GIẤY THI A4
MẪU GIỚI THIỆU CHUYỂN SINH HOẠT HỘI
Bài tập ôn tập cuối tuần lớp 2: Tuần 31
yêu cầu tài liệu
Giúp bạn tìm tài liệu chưa có
×



