
Home
Giáo án bài giảng
Giáo án, bài giảng lớp 10
BÀI TẬP HÓA HỌC :CÁC LOẠI PHẢN ỨNG TRONG HÓA HỌC VÔ CƠ
BÀI TẬP HÓA HỌC :CÁC LOẠI PHẢN ỨNG TRONG HÓA HỌC VÔ CƠ
PHÂN LOẠI PHẢN ỨNG TRONG HÓA HỌC VÔ CƠ
I. Mục tiêu:
- Phản ứng hóa hợp, phản ứng phân hủy có thể thuộc loại phản ứng oxi hóa
khử cũng có thể không thuộc loại phản ứng oxi hóa khử; phản ứng thế luôn
thuộc phản ứng oxi hóa khử; phản ứng trao đổi không phải là phản ứng oxi
hóa khử
- Nhận biết một phản ứng hoá học thuộc loại phản ứng oxi hoá - khử dựa vào
sự thay đổi số oxi hoá của các nguyên tố
- Dựa vào số oxi hóa có thể chia các phản ứng hóa học thành 2 loại chính là
phản ứng có sự thay đổi số oxi hóa và phản ứng không có sự thay đổi số oxi
hóa.
II. Trọng tâm: Phân loại các loại phản ứng.
III. Chuẩn bị:
- GV: yêu cầu hs ôn tập trước các định nghĩa phản ứng hoá hợp, phản ứng
phân huỷ, phản ứng thế, phản ứng trao đổi đã được học ở THCS
- HS: Xem trước bài ở nhà
IV. Hoạt động dạy học:
Hoạt động của giáo viên và học sinh Nội dung
Hoạt động 1:
Đn phản ứng hoá hợp?
VD1: Cho H2 tác dụng với O2 tạo H2O.
Yêu cầu học sinh viết phương trình hóa
học và xác định số oxi hóa.
VD2: Chọ CaO tác dụng với H2O viết
phương trình phản ứng và xác định số
oxi hóa. Em có nhận xét gì?
Hoạt động 2:
VD1: Phản ứng phân hủy KClO3. Viết
phương trình phản ứng và xác định số
oxi hóa.
VD2: Phản ứng nhiệt phân MgCO3.
Viết phương trình phản ứng và xác định
số oxi hóa.
Em có nhận xét gì về phản ứng phân
hủy?
I. Phản ứng có sự thay đổi số oxi hoá
và phản ứng không có sự thay đổi số
oxi hoá
1. Phản ứng hoá hợp:
- 2
2
0
H
+
0
2
O
→ 2
21
2
OH
Phản ứng có sự thay đổi số oxi hóa.
22
OCa
+
21
2
OH
→
2
122
)HO(Ca
Phản ứng không có sự thay đổi số oxi
hóa
- Trong phản ứng hóa hợp số oxi hóa
của các nguyên tố có thể thay đổi
hoặc không thay đổi
2. Phản ứng phân hủy
- 2
3
25
OClK
0
t
2
1
ClK
+ 3
0
2
O
Phản ứng có sự thay đổi số oxi hóa của
các nguyên tố.
-
3
242
OCMg
0
t
22
OMg
+
2
2
4
OC
Phản ứng không có sự thay đổi số oxi
hóa của các nguyên tố
- Trong phản ứng phân hủy, số oxi hóa
của các nguyên tố có thể thay đổi hoặc
không thay đổi.
Hoạt động 3:
VD1: Cho Cu tác dụng với AgNO3.
Viết phương trình phản ứng và xác định
số oxi hóa.
VD2: Mg tác dụng với HCl. Viết
phương trình phản ứng và xác định số
oxi hóa
Em có nhận xét gì về phản ứng thế ?
Hoạt động 4:
VD: Cho AgNO3 tác dụng với NaCl.
Viết phương trình phản ứng và xác định
số oxi hóa của các nguyên tố.
Em có nhận xét gì về phản ứng trao
đổi ?
Hoạt động 5:
- Dựa vào sự thay đổi số oxi hóa của
các nguyên tử có thể chia phản ứng hóa
học thành 2 loại được không ? vì sao?
3. Phản ứng thế
-
0
Cu
+2
3
1
NOAg
→
23
2
)NO(Cu
+ 2
0
Ag
Phản ứng có sự thay đổi số oxi hóa của
Cu và Ag.
-
0
Mg
+
ClH
1
→
2
2
ClMg
+
0
2
H
Phản ứng có sự thay đổi số oxi hóa của
các nguyên tố.
- Trong phản ứng thế bao giờ cũng có
sự thay đổi số oxi hóa của các nguyên tố
4. Phản ứng trao đổi
-
2
3
51
ONAg
+
11
ClNa
→
11
ClAg
+
3
251
ONNa
Trong phản ứng không bao giờ có sự
thay đổi số oxi hóa của các nguyên tố.
II. Kết luận
- Phản ứng hóa học có sự thay đổi số
oxi hóa là phản ứng oxi hóa khử: phản
ứng thể, 1 phần phản ứng hóa hợp và
phản ứng phân hủy;
- Phản ứng hóa học không có sự thay
đổi số oxi hóa không phải là phản ứng
oxi hóa khử: phản ứng trao đối, 1 số
phản ứng hóa hợp và phản ứng phân
hủy.
IV. Cũng cố:
- Làm bài tập 2,3,4 trong SGK
- chuẩn bị tiết sau luyện tập: xem lại lý thuyết trong chương
có thể bạn quan tâm

Luận văn: Định danh sơ bộ một loại nấm Linh chi đỏ mọc tự nhiên tại tr...
76
928
412
Kinh tế quản lý
76
(New)

Phần tìm hiểu các thuật toán phân loại văn bản, tách từ tiếng Việt, ph...
132
908
441
Kỹ thuật
132
(New)

Khảo sát một vài tính chất hóa sinh (phân tích protein, độ bền thể gel...
73
955
460
Kinh tế - Thương mại
73
(New)

Luận văn: Rủi ro, phân loại rủi ro trong các dự án đầu tư BOT
106
1.207
349
Kinh tế quản lý
106
(New)
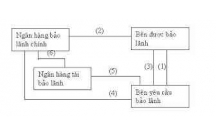
Phân loại bảo lãnh trong ngân hàng
3
727
343
Tài liệu tài chính - ngân hàng khác
3
(New)

Khảo sát, đánh giá sự phân bố các chủng vi nấm Trichoderma trong các l...
60
806
594
Khoa học tự nhiên
60
(New)

Vận Đơn Là Gì? Chức Năng, Tác Dụng & Phân Loại B/L Đường Biển trong XN...
5
1.274
463
Kế toán, kiểm toán
5
(New)
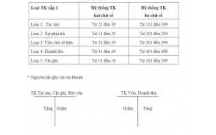
Nguyên tắc Phân loại tài sản theo dõi trong trạng thái tĩnh của kế toá...
2
617
294
Kế toán, kiểm toán
2
(New)
thông tin tài liệu
BÀI TẬP HÓA HỌC :CÁC LOẠI PHẢN ỨNG TRONG HÓA HỌC VÔ CƠ
Phản ứng có sự thay đổi số oxi hoá và phản ứng không có sự thay đổi số oxi hoá
1. Phản ứng hoá hợp:
- 2 + → 2
Phản ứng có sự thay đổi số oxi hóa.
+ →
Phản ứng không có sự thay đổi số oxi hóa
- Trong phản ứng hóa hợp số oxi hóa của các nguyên tố có thể thay đổi hoặc không thay đổi
2. Phản ứng phân hủy
- 2 2 + 3
Phản ứng có sự thay đổi số oxi hóa của các nguyên tố.
- +
Phản ứng không có sự thay đổi số oxi hóa của các nguyên tố
- Trong phản ứng phân hủy, số oxi hóa của các nguyên tố có thể thay đổi hoặc không thay đổi.
3. Phản ứng thế
- +2 → + 2
Phản ứng có sự thay đổi số oxi hóa của Cu và Ag.
- + → +
Phản ứng có sự thay đổi số oxi hóa của các nguyên tố.
- Trong phản ứng thế bao giờ cũng có sự thay đổi số oxi hóa của các nguyên tố
4. Phản ứng trao đổi
- + → +
Trong phản ứng không bao giờ có sự thay đổi số oxi hóa của các nguyên tố.
II. Kết luận
- Phản ứng h
Mở rộng để xem thêm
từ khóa liên quan
tài liệu mới trong mục này
tài liệu hot trong mục này
tài liệu giúp tôi
Nếu bạn không tìm thấy tài liệu mình cần có thể gửi yêu cầu ở đây để chúng tôi tìm giúp bạn!
xem nhiều trong tuần
70 câu hỏi trắc nghiệm luyện thi chứng chỉ tin A
Đề thi và lời giải môn xác suất thống kê của trường Học viện ngân hàng
Địa lý 12 Phát triển cây công nghiệp lâu năm Tây Nguyên
Giáo trình Quản trị học của Đại học kinh tế quốc dân
Tiểu luận: Vị trí, vai trò, nhiệm vụ của người Đảng viên với ĐCSVN- Phấn đấu, rèn luyện và tuyên truyền nhân dân của người Đảng viên
Bài tập nâng cao Tiếng Việt lớp 2: Chính tả
yêu cầu tài liệu
Giúp bạn tìm tài liệu chưa có
×



