
HÓA HỌC 8 LÝ THUYẾT VÀ BÀI TẬP AXIT – BAZƠ - MUỐI
BÀI 37: AXIT – BAZƠ - MUỐI
I. Mục tiêu:
1. Kiến thức
Biết được:
- Định nghĩa axit, bazơ, muối theo thành phần phân tử.
- Cách gọi tên axit, bazơ, muối.
- Phân loại axit, bazơ, muối.
2. Kỹ năng
- Phân loại được axit, bazơ, muối theo công thức hoá học cụ thể.
- Viết được CTHH của một số axit, bazơ, muối khi biết hoá trị của kim loại và gốc axit.
- Đọc được tên một số axit, bazơ, muối theo CTHH cụ thể và ngược lại.
-Phân biệt được một số dung dịch axit, bazơ bằng giấy quì tím.
- Tính được khối lượng một số axit, bazơ, muối tạo thành trong phản ứng.
II. Chuẩn bị
1. Giáo viên: Bảng phụ
Phiếu 1:
Công thức Tên gọi Thành phần
Nguyên tử hiđro Gốc axit
Kết luận: ……………………………………………………………………………
Phiếu 2:
Công thức Tên gọi Thành phần
Nguyên tử kim loại Nhóm hiđroxit
Kết luận: ……………………………………………………………………………
2. Học sinh: Ôn lại bài hoá trị và oxit
III. Tiến trình
1. Ổn định tổ chức
2 Kiểm tra bài cũ
- Nêu tính chất vật lý, hoá học của nước.
- Bài tập: Viết phương trình phản ứng hoá học tạo ra bazơ và axit.
3. Bài mới
a. Vào bài: Chúng ta đã làm quen với một loại hợp chất có tên gọi là oxit. Trong các hợp chất
vô cơ còn có các hợp chất khác như: Axit, bazơ, muối. Chúng là những chất như thế nào? Có
công thức hoá học và tên gọi ra sao? được phân loại như thế nào?
b. Hoạt động dạy và học:
Nội dung Hoạt động của GV, HS
I. Axit
Hoạt động 1: Axit
- GV: Treo bảng phụ, Yêu cầu 1HS
hoàn thành trên bản, ở dưới các em là
theo nhóm vào phiếu học tập.
- GV: Quan sát, nhắc nhở, gọi HS nhận
xét rồi rút ra kết luận.
- HS: Hoàn thành phiếu học tập.
- HS: Nhận xét, bổ sung.
Phiếu 1:
Tên gọi Công thức Thành phần
Nguyên tử hiđro Gốc axit
Axit clohiđric
Axit sunfuaric
Axit nitric
Axit photphoric
Axit cacbonic
HCl
H2SO4
HNO3
H3PO4
H2CO3
1 H
2 H
1 H
3 H
2 H
- Cl Clorua
= SO4 Sunfat
- NO3 Nitrat
≡ PO4 Phôtphat
= CO3 Cacbonat
Kết luận: Phân tử axit gồm một hay nhều nguyên tử hiđro liên kết với gốc axit, các nguyên tử
hiđro này có thể thay thế bằng các nguyên tử kim loại.
Hoạt động của GV Hoạt động của HS
2. Công thức hoá học:
- GV: Công thức hoá học của axit viết
tổng quát như sau: HxB
H: Nguyên tử hiđro
x: Chỉ số, chỉ số nguyên tử hiđro
B: Gốc axit
3. Phân loại:
- GV: Căn cứ vào đâu để phân loại axit?
Có mấy loại axit, lấy ví dụ minh hoạ?
4. Tên gọi
- GV: Giới thiệu hai cách gọi tên axit,
yêu cầu HS gọi tên các axit.
- HS: Nghe và ghi bài.
- HS: Dựa vào thành phần phân tử, axit
được chia thành 2 loại:
+ Axit không có oxi: HCl; H2S; HBr …
+ Axit có oxi: H2SO4; HNO3; H3PO4 …
- HS: Gọi tên các axit
- Axit không có oxi:
HCl: Axit clo hiđric
H2S: Axit sunfua hiđric
HBr: Axit brom hiđric
II. Bazơ
1. Khái niệm:
- GV: Treo bảng phụ, Yêu cầu 1HS
hoàn thành trên bản, ở dưới các em là
theo nhóm vào phiếu học tập.
- GV: Quan sát, nhắc nhở, gọi HS nhận
xét rồi rút ra kết luận.
- Axit có oxi:
HNO3: Axit nitric
H3PO4: Axit photphoric
H2CO3: Axit cacbonic
Hoạt động 2: Bazơ
- HS: Hoàn thành phiếu học tập.
- HS: Nhận xét, bổ sung.
Phiếu 2:
Công thức Tên gọi Thành phần
Nguyên tử kim loại Nhóm hiđroxit
KOH
Ba(OH)2
NaOH
Cu(OH)2
Fe(OH)3
Kali hiđroxit
Bari hiđroxit
Natri hiđroxit
Đồng (II) hiđroxit
Sắt (III) hiđroxit
1 K
1 Ba
1 Na
1 Cu
1 Fe
1 nhóm (OH)
2 nhóm (OH)
1 nhóm (OH)
2 nhóm (OH)
3 nhóm (OH)
Kết luận: Phân tử bazơ gồm có một nguyên tử kim loại liên kết với một hay nhiều nhóm
hiđroxit (- OH).
Hoạt động của GV Hoạt động của HS
2. Công thức hoá học:
- GV: Công thức hoá học của bazơ viết
tổng quát như sau: M(OH)n
M: Nguyên tử kim loại
n: Chỉ số, chỉ số nhóm hiđroxit.
(n có số trị bằng hoá trị của kim loại)
3. Tên gọi
- GV: Giới thiệu cách gọi tên bazơ, yêu
cầu HS gọi tên các bazơ.
NaOH: Natri hiđroxit
Cu(OH)2: Đồng (II) hiđroxit
Fe(OH)3: Sắt (III) hiđroxit
4. Phân loại:
- GV: Căn cứ vào đâu để phân loại
bazơ? Có mấy loại bazơ, lấy ví dụ minh
hoạ?
- HS: Nghe và ghi bài.
- HS: Gọi tên các bazơ
NaOH: Natri hiđroxit
Cu(OH)2: Đồng (II) hiđroxit
Fe(OH)3: Sắt (III) hiđroxit
- HS: Dựa vào tính tan, bazơ được chia
thành 2 loại:
+ Bazơ tan: KOH; Ba(OH)2; NaOH
+ Bazơ không tan: Cu(OH)2; Fe(OH)3
Nội dung ghi bảng
Axit Bazơ Muối
Ví dụ HCl, H2SO4NaOH, Cu(OH)2
Định nghĩa
Phân tử axit gồm một
hay nhều nguyên tử
hiđro liên kết với gốc
axit, các nguyên tử hiđro
này có thể thay thế
bằng
các nguyên tử kim loại.
Phân tử bazơ gồm có
một nguyên tử kim
loại liên kết với một
hay nhiều nhóm
hiđroxit (- OH).
CTHH
HxB. Trong đó:
H: Nguyên tử hiđro
x: Chỉ số, chỉ số nguyên
tử hiđro
B: Gốc axit
M(OH)n. Trong đó:
M: Nguyên tử kim
loại
n: Chỉ số, chỉ số
nhóm hiđroxit.
Phân loại
và tên gọi
Dựa vào thành phần
phân tử, axit được chia
thành 2 loại:
- Axit không có oxi:
HCl: axit clohiđric
H2S: axit sunfuhiđric
- Axit có oxi:
H2SO4: Axit sunfuric
HNO3: axit nitric
H3PO4: Axit photphoric
Dựa vào tính tan,
bazơ được chia
thành 2 loại:
- Bazơ tan:
KOH: Kali hiđroxit
Ba(OH)2: Bari
hiđroxit
- Bazơ không tan:
Cu(OH)2: Đồng (II)
hiđroxit
Fe(OH)3: Sắt (III)
hiđroxit
IV. Luyện tập, củng cố
- GV yêu cầu HS trả lời bài 1. HS trả lời
- Bài 1: Lập CTHH của axit biết gốc axit – Br, = CO3. Phân loại, gọi tên.
- Bài 2: Viết CTHH bazơ của các kim loại Al (III), Ca (II). Phân loại và tên gọi.
- Bài 3: Trung hoà 300 ml dung dịch HCl 0,1 M bằng dung dịch NaOH. Tính khối lượng muối
sinh ra sau phản ứng.
Giải:
Số mol HCl tham gia phản ứng là 0,1 . 0,3 = 0,03 (mol)
PTHH: HCl + NaOH
NaCl + H2O
1 mol 1 mol
0,03 mol 0,03 mol
có thể bạn quan tâm

Tóm tắt kiến thức cơ bản và giải bài tập Hóa học lớp 11: Axit, bazơ và...
3
1.089
345
Giải bài tập các môn
3
(New)

HÓA HỌC : THỰC HÀNH BAZƠ VÀ MUỐI
2
830
371
Giáo án, bài giảng lớp 9
2
(New)

Hướng dẫn giải bài tập Hóa học 9 - Thực hành: Tính chất hóa học của ba...
2
869
346
Giải bài tập các môn
2
(New)

Tóm tắt kiến thức cơ bản và giải bài tập Hóa học lớp 11: Sự điện li củ...
3
819
338
Giải bài tập các môn
3
(New)

HÓA HỌC TÌM HIỂU VỀ AXIT SUNFURIC, MUỐI SUNFAT (T2)
2
1.218
388
Giáo án, bài giảng lớp 10
2
(New)

HÓA HỌC TÌM HIỂU VỀ AXIT SUNFURIC, MUỐI SUNFAT (T3)
2
1.095
381
Giáo án, bài giảng lớp 10
2
(New)
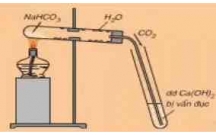
Giải bài tập Hóa Học 9: Axit cacbonic và muối cacbonat
2
938
447
Giải bài tập các môn
2
(New)

Tóm tắt kiến thức cơ bản và Giải bài tập Hóa học lớp 11: Axit nitric v...
4
772
322
Giải bài tập các môn
4
(New)
thông tin tài liệu
HÓA HỌC 8 LÝ THUYẾT VÀ BÀI TẬP AXIT – BAZƠ - MUỐI
Axit Bazơ Muối
Ví dụ HCl, H2SO4 NaOH, Cu(OH)2 NaCl, BaSO4
Định nghĩa Phân tử axit gồm một hay nhều nguyên tử hiđro liên kết với gốc axit, các nguyên tử hiđro này có thể thay thế bằng các nguyên tử kim loại. Phân tử bazơ gồm có một nguyên tử kim loại liên kết với một hay nhiều nhóm hiđroxit (- OH).
Phân tử muối gồm một hay nhiều nguyên tử kim loại liên kết với một hay nhiều gốc axit.
CTHH HxB. Trong đó:
H: Nguyên tử hiđro
x: Chỉ số, chỉ số nguyên tử hiđro
B: Gốc axit M(OH)n. Trong đó: M: Nguyên tử kim loại
n: Chỉ số, chỉ số nhóm hiđroxit. AxBy. Trong đó:
A: Nguyên tử kim loại
B: Gốc axit
x, y: Chỉ số
Phân loại và tên gọi Dựa vào thành phần phân tử, axit được chia thành 2 loại:
- Axit không có oxi:
HCl: axit clohiđric
H2S: axit sunfuhiđric
- Axit có oxi:
H2SO4: Axit sunfuric HNO3: axit nitric
H3PO4: Axit photphoric Dựa vào tính tan, bazơ được chia thành 2 loại:
- Bazơ tan:
KOH: Kali hiđroxit Ba(OH)2: Bari hiđroxit
- Bazơ không tan: Cu(OH)2: Đồng (II) hiđroxit
Fe(OH)3: Sắt (III) hiđroxit Dựa vào thành phần phân tử, muối được chia thành hai loại:
a) Muối trung hoà: Na2CO3: natri cacbonat
K2SO4: Kali sunfat
b) Muối axit: NaHCO3: Natri hiđro cacbonat KHCO3: Kali hiđro cacbonat
Mở rộng để xem thêm
từ khóa liên quan
tài liệu mới trong mục này
tài liệu hot trong mục này
tài liệu giúp tôi
Nếu bạn không tìm thấy tài liệu mình cần có thể gửi yêu cầu ở đây để chúng tôi tìm giúp bạn!
xem nhiều trong tuần
Địa lý 12 Phát triển cây công nghiệp lâu năm Tây Nguyên
Đề thi và lời giải môn xác suất thống kê của trường Học viện ngân hàng
Giáo trình Quản trị học của Đại học kinh tế quốc dân
MẪU GIẤY THI A4
MẪU GIỚI THIỆU CHUYỂN SINH HOẠT HỘI
Bài tập ôn tập cuối tuần lớp 2: Tuần 31
yêu cầu tài liệu
Giúp bạn tìm tài liệu chưa có
×



